Đánh giá độ an toàn của Tenofovir disoproxil fumarate ở phụ nữ mang thai và đang cho con bú trong điều trị HBV mạn tính
- Cơ chế tác dụng của Tenofovir disoproxil fumarate
- Nồng độ Tenofovir disoproxil fumarate trong sữa mẹ và ở trẻ bú mẹ
- Tác dụng không mong muốn ở trẻ bú mẹ
- Ảnh hưởng của Tenofovir disoproxil fumarate (TDF) đối với trẻ khi mẹ sử dụng trong thai kỳ
- Khuyến nghị của các tổ chức quốc tế về sử dụng Tenofovir disoproxil fumarate cho phụ nữ mang thai và cho con bú
- Kết luận
- Câu hỏi thường gặp về Tenofovir disoproxil fumarate ở phụ nữ mang thai
Viêm gan B mạn tính là một trong những bệnh truyền nhiễm phổ biến nhất trên thế giới. Theo Tổ chức Y tế Thế giới (WHO), hiện nay có hơn 296 triệu người đang sống chung với virus viêm gan B (HBV) và mỗi năm có khoảng 1,5 triệu ca nhiễm mới. Trong số đó, một tỷ lệ đáng kể là phụ nữ trong độ tuổi sinh sản. Đối với phụ nữ mang thai mắc HBV mạn tính, mối lo lớn nhất không chỉ là sức khỏe của bản thân mà còn là nguy cơ lây truyền virus từ mẹ sang con. Nếu không có biện pháp dự phòng thích hợp, tỷ lệ lây truyền dọc có thể lên tới 90% ở những bà mẹ có tải lượng virus cao. Trẻ sơ sinh nhiễm HBV từ mẹ thường có nguy cơ cao tiến triển thành viêm gan B mạn tính suốt đời, kéo theo nhiều biến chứng nguy hiểm như xơ gan hoặc ung thư gan sau này. Trong bối cảnh đó, Tenofovir disoproxil fumarate (TDF) đã trở thành một trong những thuốc kháng virus được sử dụng rộng rãi nhất để kiểm soát HBV. Thuốc không chỉ có hiệu quả mạnh trong việc ức chế virus mà còn được nhiều tổ chức y khoa quốc tế khuyến cáo sử dụng cho phụ nữ mang thai có nguy cơ lây truyền cao.
Tuy nhiên, nhiều bệnh nhân vẫn đặt ra những câu hỏi quan trọng: Tenofovir disoproxil fumarate có an toàn cho thai nhi không? Phụ nữ đang mang thai có nên tiếp tục dùng thuốc không? Nếu đang điều trị Tenofovir thì có thể cho con bú không? Bài viết dưới đây, Thuốc Viêm Gan sẽ phân tích độ an toàn của Tenofovir disoproxil fumarate ở phụ nữ mang thai và đang cho con bú, dựa trên các nghiên cứu khoa học, khuyến cáo của các hiệp hội gan mật.
Cơ chế tác dụng của Tenofovir disoproxil fumarate
Tenofovir là một chất tương tự nucleotide của adenosine 5’-monophosphate, thuộc nhóm thuốc kháng virus được sử dụng rộng rãi trong điều trị viêm gan B mạn tính. Ở dạng nguyên thủy, tenofovir tồn tại dưới dạng dianion tại pH sinh lý, do đó khả năng đi qua màng tế bào khá kém và sinh khả dụng khi dùng đường uống không cao.
Để khắc phục hạn chế này, hoạt chất được phát triển dưới dạng tiền chất Tenofovir disoproxil fumarate (TDF). Khi được uống vào cơ thể, TDF nhanh chóng được hấp thu và chuyển hóa trong máu thành tenofovir. Sau đó, tenofovir tiếp tục đi vào tế bào và được phosphoryl hóa thành dạng hoạt động là tenofovir diphosphate.
Dạng hoạt hóa này đóng vai trò quan trọng trong việc ức chế sự nhân lên của virus. Tenofovir diphosphate cạnh tranh trực tiếp với deoxyadenosine triphosphate (dATP) – một nucleotide tự nhiên cần thiết cho quá trình tổng hợp DNA của virus viêm gan B. Khi tenofovir được tích hợp vào chuỗi DNA đang hình thành của virus, cấu trúc của nó khiến các nucleotide tiếp theo không thể gắn thêm vào chuỗi. Hệ quả là quá trình kéo dài chuỗi DNA bị chặn lại, gây kết thúc chuỗi DNA sớm.
Nhờ cơ chế này, Tenofovir disoproxil fumarate giúp ức chế hiệu quả quá trình sao chép của virus HBV, từ đó làm giảm tải lượng virus trong cơ thể và hỗ trợ kiểm soát tiến triển của bệnh viêm gan B mạn tính.
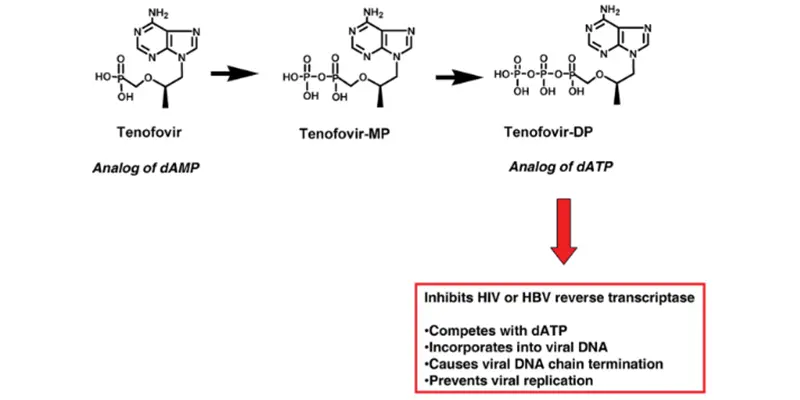
Sơ đồ mô tả hoạt hóa nội bào và cơ chế tác dụng kháng virus của tenofovir
Nồng độ Tenofovir disoproxil fumarate trong sữa mẹ và ở trẻ bú mẹ
Nồng độ Tenofovir disoproxil fumarate trong sữa mẹ
Các nghiên cứu hiện nay cho thấy lượng Tenofovir disoproxil fumarate (TDF) bài tiết vào sữa mẹ rất thấp. Sinh khả dụng của tenofovir đối với trẻ bú mẹ chưa được xác định chính xác, tuy nhiên nhiều bằng chứng cho thấy khả năng hấp thu qua sữa mẹ gần như không đáng kể.
Trong một nghiên cứu trên 11 phụ nữ mắc viêm gan B mạn tính sử dụng TDF liều 245 mg mỗi ngày trong ít nhất 1 tháng, các mẫu sữa mẹ được thu thập trung bình 12 giờ sau khi dùng thuốc (dao động 10–17 giờ). Kết quả cho thấy nồng độ tenofovir trung bình trong sữa mẹ khoảng 6,69 mcg/L, với khoảng giá trị từ 4,887 mcg/L đến 7,03 mcg/L.
Một nghiên cứu khác thực hiện trên 13 bà mẹ dùng Tenofovir disoproxil fumarate 300 mg mỗi ngày đã thu thập 24 mẫu sữa mẹ, trung bình 16 giờ sau khi uống thuốc. Nồng độ thuốc đo được trong sữa khoảng 5 mcg/L. Từ dữ liệu này, các nhà nghiên cứu ước tính trẻ sơ sinh bú mẹ sẽ nhận được khoảng 1 mcg/kg/ngày, tương đương 0,01% liều điều chỉnh theo cân nặng của người mẹ – mức rất thấp về mặt lâm sàng.
Ngoài ra, một nghiên cứu lớn hơn trên 30 phụ nữ mang thai mắc viêm gan B được điều trị bằng Tenofovir disoproxil fumarate 300 mg mỗi ngày từ tuần thai 24–32 cho đến 3 tháng sau sinh cũng cung cấp thêm dữ liệu quan trọng.
Các mẫu sữa được thu thập tại nhiều thời điểm sau khi dùng thuốc. Trong tổng số 81 mẫu sữa, nồng độ tenofovir cao nhất ghi nhận được là 14,5 mcg/L vào ngày đầu sau khi uống thuốc. Nồng độ trung bình tại các mốc thời gian:
- 24 giờ sau liều cuối: khoảng 4 mcg/L
- 48 giờ: khoảng 2 mcg/L
- 72 giờ: khoảng 1,1 mcg/L
So sánh với nồng độ thuốc trong cơ thể người mẹ cho thấy lượng tenofovir trong sữa chỉ tương đương 11,6% nồng độ trong huyết tương và 1% nồng độ trong nước ối. Theo ước tính của nhóm nghiên cứu, một trẻ bú mẹ hoàn toàn chỉ tiếp nhận khoảng 0,21–1,76 mcg/kg/ngày, tương đương 0,029% liều điều trị đường uống khuyến cáo cho trẻ em.
Nồng độ Tenofovir disoproxil fumarate ở trẻ bú mẹ
Không chỉ nồng độ trong sữa thấp, nhiều nghiên cứu còn cho thấy tenofovir hầu như không phát hiện được trong máu trẻ bú mẹ.
Trong một nghiên cứu nhỏ, 5 trẻ sơ sinh được nuôi bằng sữa mẹ từ các bà mẹ dùng Tenofovir disoproxil fumarate 300 mg mỗi ngày đã được xét nghiệm nồng độ thuốc trong huyết thanh ở thời điểm 2–19 giờ sau khi mẹ uống thuốc, khi trẻ khoảng 1 tháng tuổi. Kết quả cho thấy không phát hiện được tenofovir trong huyết thanh trẻ.
Một nghiên cứu khác trên 11 bà mẹ mắc viêm gan B mạn tính đang điều trị TDF, trong đó 7 trẻ được bú mẹ hoàn toàn, cũng cho kết quả tương tự. Mẫu máu của trẻ được lấy khoảng 12 giờ sau khi mẹ uống thuốc, khi trẻ có độ tuổi trung bình 3 tháng. Tất cả các mẫu đều cho thấy nồng độ tenofovir trong huyết tương dưới ngưỡng phát hiện (<4 mcg/L).
| Nghiên cứu | Số mẹ tham gia | Liều TDF mẹ uống | Thời điểm lấy mẫu sữa | Nồng độ TDF trong sữa mẹ | Liều ước tính trẻ bú nhận | Ghi chú |
| Nghiên cứu 1 | 11 mẹ | 245 mg/ngày (≥1 tháng) | ~12h sau uống (10–17h) | TB: 6,69 mcg/L (4,88–7,03) |
Không tính trực tiếp |
Mẫu đơn, nồng độ ổn định thấp |
| Nghiên cứu 2 | 13 mẹ | 300 mg/ngày | ~16h sau uống | TB: 5 mcg/L | ~1mcg/kg/ngày (~0,01% liều mẹ) | Phơi nhiễm của bé rất thấp |
| Nghiên cứu 3 | 30 mẹ | 300 mg/ngày (từ tuần 24–32 thai kỳ → 3 tháng sau sinh) | Nhiều thời điểm (0,5h–72h sau uống) |
Cao nhất: 14,5 mcg/L TB: 24h = 4 mcg/L, 48h = 2 mcg/L, 72h = 1,1 mcg/L |
0,21 – 1,76 mcg/kg/ngày (~0,029% liều trẻ em) | So với máu mẹ: sữa chỉ chứa ~11,6%; so với nước ối: chỉ 1% |
Tác dụng không mong muốn ở trẻ bú mẹ
Nhiều nghiên cứu lâm sàng đã được thực hiện nhằm đánh giá mức độ an toàn của tenofovir disoproxil fumarate (TDF) khi sử dụng cho phụ nữ mang thai và đang cho con bú. Các nghiên cứu này chủ yếu theo dõi sự phát triển thể chất, thần kinh cũng như các phản ứng bất lợi có thể xảy ra ở trẻ sơ sinh bú sữa mẹ. Kết quả tổng hợp cho thấy phần lớn các trường hợp không ghi nhận bất thường đáng kể ở trẻ bú mẹ.
Một nghiên cứu trên 30 phụ nữ mắc viêm gan B cho thấy các thai phụ được điều trị TDF liều 300 mg mỗi ngày, bắt đầu từ tuần thứ 24–32 của thai kỳ và tiếp tục trong 3 tháng sau sinh. Trong thời gian này, trẻ vẫn được bú sữa mẹ (không xác định rõ mức độ). Theo dõi trong suốt quá trình điều trị không ghi nhận dấu hiệu hay triệu chứng bất thường ở trẻ. Các chỉ số tăng trưởng như chiều cao, cân nặng và vòng đầu được đánh giá tại thời điểm sinh, 3 tháng, 6 tháng và 12 tháng tuổi đều nằm trong giới hạn bình thường theo tiêu chuẩn phát triển.
Ở một báo cáo khác, hai trẻ sơ sinh có mẹ sử dụng TDF 300 mg/ngày được bú mẹ hoàn toàn trong 3 tháng đầu đời. Khi được 4 tháng tuổi, cả hai trẻ đều phát triển bình thường, không xuất hiện bất kỳ dấu hiệu bất lợi nào liên quan đến sự tăng trưởng hoặc sức khỏe tổng thể.
Một nghiên cứu nhỏ trên 5 phụ nữ nhiễm viêm gan B được điều trị TDF 300 mg/ngày từ tam cá nguyệt thứ ba và tiếp tục sau sinh cũng ghi nhận kết quả tương tự. Mặc dù ban đầu được khuyến cáo không cho con bú, cả 5 bà mẹ vẫn nuôi con bằng sữa mẹ (không xác định rõ mức độ). Trong quá trình theo dõi ngắn hạn, không ghi nhận phản ứng phụ ở trẻ sơ sinh, đồng thời xét nghiệm HBsAg của các trẻ đều âm tính khi kiểm tra ở giai đoạn 28–36 tuần tuổi.
Một nghiên cứu khác theo dõi 14 phụ nữ điều trị viêm gan B bằng TDF trong thai kỳ (trong đó 12 trường hợp bắt đầu từ tam cá nguyệt thứ nhất). Trong nhóm này, có 3 bà mẹ cho con bú trong thời gian dùng thuốc. Các trẻ được theo dõi đến 1 tuổi và không ghi nhận bất kỳ tác dụng bất lợi nào liên quan đến việc bú sữa mẹ.
Tương tự, trong một nghiên cứu dài hạn về hiệu quả và độ an toàn của TDF trong điều trị viêm gan B mạn tính, có 3 phụ nữ tiếp tục cho con bú trong khi điều trị. Kết quả theo dõi đến khi trẻ tròn 1 tuổi cho thấy không có trường hợp nào gặp phản ứng bất lợi.
Đáng chú ý, một nghiên cứu quy mô lớn hơn tại Trung Quốc trên 143 phụ nữ mang thai nhiễm viêm gan B cho thấy TDF 300 mg/ngày được sử dụng từ tuần 22–33 của thai kỳ và tiếp tục sau sinh. Trong số này có 31 bà mẹ cho con bú (không xác định mức độ) đồng thời trẻ được thực hiện đầy đủ các biện pháp dự phòng viêm gan B tiêu chuẩn. Khi đánh giá tại tuần thứ 28 sau sinh, sự phát triển thể chất và thần kinh của trẻ đều nằm trong giới hạn tiêu chuẩn quốc gia, và không có trẻ nào bị lây nhiễm viêm gan B.
Một số triệu chứng nhẹ được ghi nhận ở hơn 5% trẻ như ho hoặc sốt. Các biểu hiện ít gặp hơn bao gồm phát ban da, tiêu chảy, nôn, vàng da và viêm phổi. Tuy nhiên, các nhà nghiên cứu kết luận rằng những tác dụng này không liên quan đến việc người mẹ sử dụng TDF.
Nhìn chung, các dữ liệu hiện có cho thấy việc sử dụng TDF ở phụ nữ mang thai và cho con bú không gây ảnh hưởng đáng kể đến sức khỏe và sự phát triển của trẻ bú mẹ, đặc biệt khi trẻ được theo dõi và chăm sóc theo đúng khuyến cáo y khoa.
Ảnh hưởng của Tenofovir disoproxil fumarate (TDF) đối với trẻ khi mẹ sử dụng trong thai kỳ
Khả năng qua nhau thai của Tenofovir disoproxil fumarate
Tenofovir disoproxil fumarate (TDF) có khả năng đi qua hàng rào nhau thai và tiếp cận thai nhi trong quá trình mang thai. Các nghiên cứu dược động học cho thấy mức độ truyền thuốc từ mẹ sang thai nhi khá cao. Tỷ lệ nồng độ tenofovir trong máu cuống rốn so với huyết tương của mẹ tại thời điểm sinh thường lớn hơn 0,6. Ở những phụ nữ mang thai điều trị TDF kéo dài, tỷ lệ này dao động trong khoảng 0,60 – 1,03.
Chính vì đặc điểm này, vấn đề an toàn của Tenofovir disoproxil fumarate đối với thai nhi vẫn được giới chuyên môn quan tâm, đặc biệt liên quan đến các yếu tố như tăng trưởng chiều cao, chức năng thận và sự phát triển của hệ xương. Tuy nhiên, nhiều bằng chứng hiện nay cho thấy việc mẹ sử dụng TDF trong thai kỳ không làm gia tăng nguy cơ các rối loạn về chuyển hóa, tăng trưởng, phát triển tim mạch hay thần kinh ở trẻ sơ sinh.
Trong điều trị viêm gan B mạn tính ở phụ nữ mang thai, Tenofovir disoproxil fumarate hiện được xem là lựa chọn ưu tiên nhằm giảm nguy cơ lây truyền virus HBV từ mẹ sang con. Thuốc được đánh giá cao nhờ hiệu quả kiểm soát virus tốt và hồ sơ an toàn tương đối ổn định. Tuy vậy, dữ liệu về ảnh hưởng lâu dài đối với trẻ từng tiếp xúc với TDF trong giai đoạn bào thai vẫn đang tiếp tục được nghiên cứu.
Một nghiên cứu theo dõi dài hạn tại Đài Loan về phòng ngừa lây truyền HBV từ mẹ sang con đã đánh giá sự tăng trưởng và sức khỏe xương của trẻ có mẹ sử dụng TDF trong thai kỳ. Nghiên cứu bao gồm 128 trẻ, trong đó 71 trẻ thuộc nhóm có mẹ điều trị Tenofovir disoproxil fumarate và 57 trẻ thuộc nhóm đối chứng. Các trẻ được theo dõi từ 2 đến 7 tuổi với tổng cộng 255 lần tái khám.
Kết quả cho thấy không có sự khác biệt đáng kể giữa hai nhóm về chỉ số cân nặng, chiều cao cũng như mức lọc cầu thận ước tính theo độ tuổi. Khi phân tích sâu hơn bằng phương pháp hồi quy tuyến tính và điều chỉnh các yếu tố như tuổi, giới tính và tình trạng nhiễm HBV, các chỉ số sinh hóa liên quan đến chuyển hóa xương như canxi huyết thanh, phốt pho, phosphatase kiềm đặc hiệu xương, calcidiol đều tương đương giữa hai nhóm.
Ngoài ra, mật độ khoáng xương tại cột sống thắt lưng và vùng hông trái của trẻ trong nhóm tiếp xúc với Tenofovir disoproxil fumarate cũng không khác biệt so với nhóm đối chứng trong suốt thời gian theo dõi 6–7 năm sau sinh.
Sự phát triển về thể chất và thần kinh ở thai nhi
Một nghiên cứu được thực hiện tại Trung Quốc đã đánh giá tác động lâu dài của Tenofovir disoproxil fumarate (TDF) đối với sự phát triển thể chất và thần kinh của trẻ sinh ra từ các bà mẹ mắc viêm gan B mạn tính. Mục tiêu của nghiên cứu là xem liệu việc sử dụng thuốc trong tam cá nguyệt thứ ba nhằm phòng ngừa lây truyền HBV từ mẹ sang con có ảnh hưởng đến sức khỏe và sự phát triển của trẻ hay không.
Nghiên cứu này là giai đoạn theo dõi dài hạn của một thử nghiệm ngẫu nhiên có đối chứng trước đó. Trong thử nghiệm ban đầu, các thai phụ mắc viêm gan B mạn tính được chia ngẫu nhiên thành hai nhóm: một nhóm được điều trị bằng Tenofovir disoproxil fumarate trong tam cá nguyệt thứ ba, trong khi nhóm còn lại không sử dụng thuốc. Sau khi trẻ được sinh ra, các nhà nghiên cứu tiếp tục theo dõi sự phát triển của trẻ trong thời gian dài.
Các chỉ số được đánh giá bao gồm: sự phát triển thể chất, nguy cơ dị tật bẩm sinh, mật độ khoáng xương (BMD) và sự phát triển thần kinh. Đặc biệt, khả năng phát triển thần kinh của trẻ được đo lường bằng thang đánh giá Bayley-III – một công cụ tiêu chuẩn thường dùng để đánh giá nhận thức, vận động và hành vi của trẻ nhỏ. Việc theo dõi được thực hiện đến tuần thứ 192 sau sinh.
Trong tổng số 180 trẻ đủ điều kiện tham gia nghiên cứu, có 145 trẻ hoàn tất giai đoạn theo dõi dài hạn, tương đương 82%. Trong đó, nhóm đối chứng có 75 trẻ và nhóm có mẹ sử dụng Tenofovir disoproxil fumarate có 70 trẻ. Thời gian trung bình thai nhi tiếp xúc với thuốc trong tử cung là khoảng 8,57 ± 0,53 tuần.
Kết quả cho thấy tỷ lệ dị tật bẩm sinh giữa hai nhóm không có sự khác biệt đáng kể. Trọng lượng trung bình của trẻ trong cả hai nhóm đều nằm trong giới hạn bình thường khi so sánh với tiêu chuẩn quốc gia. Bên cạnh đó, các chỉ số khác như chu vi vòng đầu, chiều cao, mật độ khoáng xương và các thang đánh giá phát triển thần kinh (bao gồm nhận thức, vận động, cảm xúc – xã hội và khả năng thích nghi) cũng tương đương giữa hai nhóm.
Những dữ liệu này cho thấy trẻ từng tiếp xúc với Tenofovir disoproxil fumarate trong giai đoạn bào thai vẫn có sự phát triển thể chất, mật độ xương và chức năng thần kinh bình thường khi được theo dõi đến 192 tuần tuổi. Kết quả nghiên cứu góp phần củng cố bằng chứng khoa học về tính an toàn lâu dài của liệu pháp TDF trong việc phòng ngừa lây truyền viêm gan B từ mẹ sang con.
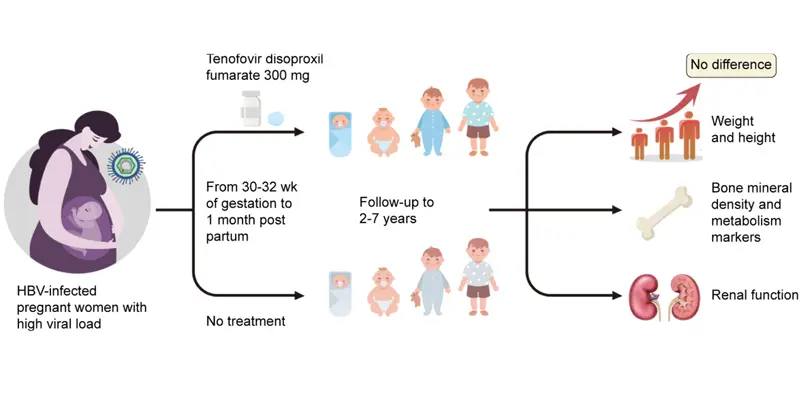
Sự phát triển về chiều cao, xương, chức năng thận ở trẻ
Khuyến nghị của các tổ chức quốc tế về sử dụng Tenofovir disoproxil fumarate cho phụ nữ mang thai và cho con bú
Khuyến cáo từ hướng dẫn AASLD 2018
Theo hướng dẫn của Hiệp hội Nghiên cứu Bệnh gan Hoa Kỳ (AASLD) năm 2018, tất cả phụ nữ mang thai cần được xét nghiệm HBsAg trong quá trình chăm sóc tiền sản nhằm phát hiện sớm tình trạng nhiễm virus viêm gan B. Đối với những trường hợp mắc viêm gan B mạn tính, thai phụ nên được tư vấn đầy đủ bởi bác sĩ chuyên khoa sản và bác sĩ nhi khoa để xây dựng chiến lược phòng ngừa lây truyền virus từ mẹ sang con.
AASLD khuyến nghị xem xét điều trị kháng virus trong tam cá nguyệt thứ ba cho các thai phụ có tải lượng HBV DNA trong huyết thanh trên 200.000 IU/mL. Việc điều trị trong giai đoạn này giúp làm giảm đáng kể nguy cơ lây nhiễm HBV cho trẻ trong thời điểm sinh nở.
Hiện nay, ba loại thuốc kháng virus đã được nghiên cứu tương đối đầy đủ trên phụ nữ mang thai gồm lamivudine, telbivudine và Tenofovir disoproxil fumarate. Trong số đó, Tenofovir disoproxil fumarate thường được ưu tiên lựa chọn nhờ hiệu quả ức chế virus mạnh và nguy cơ xuất hiện kháng thuốc thấp hơn so với các thuốc còn lại. Nhiều nghiên cứu cho thấy thuốc có khả năng làm giảm đáng kể tỷ lệ lây truyền HBV từ mẹ sang con khi được sử dụng đúng chỉ định.
Trong phần lớn các nghiên cứu lâm sàng, liệu pháp kháng virus với Tenofovir disoproxil fumarate thường được bắt đầu vào khoảng tuần thai thứ 28–32, thời điểm được xem là phù hợp để kiểm soát tải lượng virus trước khi sinh.
Đối với việc cho con bú, các hướng dẫn hiện tại không xem đây là chống chỉ định khi người mẹ đang điều trị bằng Tenofovir disoproxil fumarate. Thuốc chỉ được bài tiết vào sữa mẹ với lượng rất nhỏ và chưa ghi nhận nguy cơ gây độc tính đáng kể cho trẻ sơ sinh. Tuy nhiên, các bác sĩ vẫn cần tư vấn cho người mẹ về khả năng phơi nhiễm thuốc ở mức rất thấp đối với trẻ, mặc dù những ảnh hưởng lâu dài hiện vẫn chưa được xác định đầy đủ.
Khuyến cáo của WHO 2024 về sử dụng Tenofovir disoproxil fumarate trong thai kỳ
Khuyến nghị cập nhật
Theo Tổ chức Y tế Thế giới (WHO) năm 2024, việc dự phòng lây truyền virus viêm gan B từ mẹ sang con (MTCT) cần được triển khai sớm ở những phụ nữ mang thai có nguy cơ cao. Tại các cơ sở y tế có khả năng xét nghiệm HBV DNA hoặc HBeAg, WHO khuyến cáo sử dụng Tenofovir disoproxil fumarate để dự phòng cho tất cả thai phụ có HBsAg dương tính và có tải lượng HBV DNA ≥ 200.000 IU/mL hoặc HBeAg dương tính.
Liệu pháp dự phòng bằng Tenofovir disoproxil fumarate nên được bắt đầu từ tam cá nguyệt thứ hai của thai kỳ, và tiếp tục ít nhất đến thời điểm sinh hoặc cho đến khi trẻ sơ sinh hoàn thành đầy đủ lịch tiêm vắc-xin viêm gan B. Đây là khuyến cáo mạnh mẽ của WHO, dựa trên các bằng chứng khoa học có độ tin cậy trung bình, cho thấy hiệu quả rõ rệt trong việc giảm nguy cơ lây truyền virus sang trẻ.
Khuyến nghị mới trong bối cảnh hạn chế xét nghiệm
Ở nhiều khu vực trên thế giới, việc tiếp cận các xét nghiệm chuyên sâu như HBV DNA hoặc HBeAg vẫn còn hạn chế. Trong những trường hợp này, WHO đưa ra khuyến nghị linh hoạt hơn: có thể cân nhắc dự phòng bằng Tenofovir disoproxil fumarate cho tất cả phụ nữ mang thai có HBsAg dương tính, ngay cả khi chưa xác định được tải lượng virus.
Tương tự như khuyến cáo chính, thuốc nên được sử dụng từ tam cá nguyệt thứ hai cho đến sau khi sinh hoặc cho đến khi trẻ hoàn thành phác đồ vắc-xin viêm gan B. Tuy nhiên, đây là khuyến nghị có điều kiện, do mức độ bằng chứng hiện tại còn hạn chế.
Lưu ý đối với phụ nữ trong độ tuổi sinh sản
WHO cũng nhấn mạnh rằng đối với những phụ nữ đang trong độ tuổi sinh đẻ và có kế hoạch mang thai trong tương lai, việc sử dụng Tenofovir disoproxil fumarate không chỉ giới hạn trong một lần mang thai. Trong nhiều trường hợp, liệu pháp này có thể được:
- Tiếp tục sau sinh,
- Duy trì trong các lần mang thai tiếp theo,
- Hoặc sử dụng lâu dài như một liệu pháp điều trị viêm gan B mạn tính nếu có chỉ định.
Việc duy trì điều trị giúp kiểm soát tải lượng virus ổn định và giảm nguy cơ lây truyền HBV cho trẻ trong các lần mang thai sau.
Chiến lược dự phòng theo khả năng tiếp cận xét nghiệm
Tùy thuộc vào điều kiện của hệ thống y tế, WHO đề xuất hai hướng tiếp cận:
- Khi có xét nghiệm HBV DNA hoặc HBeAg: Dự phòng bằng Tenofovir disoproxil fumarate cho phụ nữ mang thai HBsAg dương tính có HBV DNA ≥ 200.000 IU/mL hoặc HBeAg dương tính.
- Khi không có xét nghiệm HBV DNA hoặc HBeAg: Có thể dự phòng bằng Tenofovir disoproxil fumarate cho tất cả thai phụ có HBsAg dương tính nhằm giảm nguy cơ lây truyền virus từ mẹ sang con.
Độ an toàn của Tenofovir disoproxil fumarate đối với trẻ sơ sinh
Các nghiên cứu lâm sàng đã đánh giá tính an toàn của Tenofovir disoproxil fumarate đối với trẻ sinh ra từ những bà mẹ sử dụng thuốc trong thai kỳ. Một thử nghiệm ngẫu nhiên có đối chứng (RCT) đã so sánh nhóm sử dụng thuốc dự phòng với nhóm giả dược và theo dõi mật độ khoáng xương của trẻ sơ sinh.
Kết quả cho thấy không có sự khác biệt có ý nghĩa thống kê về mật độ khoáng xương cột sống thắt lưng ở trẻ khi 1 tuổi, cho thấy thuốc không gây ảnh hưởng đáng kể đến sự phát triển xương của trẻ.
Ngoài ra, Tenofovir disoproxil fumarate được bài tiết vào sữa mẹ với nồng độ rất thấp. Cho đến nay, chưa có bằng chứng cho thấy thuốc gây độc tính cho trẻ bú mẹ. Vì vậy, phụ nữ đang điều trị bằng Tenofovir disoproxil fumarate vẫn có thể cho con bú nếu không có chống chỉ định khác.
Về phân loại an toàn thuốc trong thai kỳ, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) xếp Tenofovir disoproxil fumarate vào nhóm B, nghĩa là các nghiên cứu hiện tại không ghi nhận bằng chứng đầy đủ về nguy cơ gây hại cho thai nhi ở người.
Xem thêm
Kết luận
Nhìn chung, Tenofovir disoproxil fumarate (TDF) chỉ được bài tiết vào sữa mẹ với hàm lượng rất nhỏ. Các nghiên cứu hiện nay cho thấy nồng độ này thấp và chưa ghi nhận gây độc tính đáng kể đối với trẻ bú mẹ. Mặc dù thông tin trong tờ hướng dẫn sử dụng thuốc thường khuyến cáo thận trọng khi cho con bú trong thời gian dùng TDF, nhiều dữ liệu lâm sàng đã cho thấy thuốc có hồ sơ an toàn tốt khi sử dụng cho phụ nữ trong thai kỳ và giai đoạn nuôi con bằng sữa mẹ. Trong thực hành điều trị, việc sử dụng Tenofovir disoproxil fumarate ở phụ nữ mang thai – đặc biệt trong tam cá nguyệt thứ ba – đã được chứng minh giúp giảm đáng kể nguy cơ lây truyền virus viêm gan B từ mẹ sang con, nhất là ở những trường hợp có tải lượng HBV DNA cao. Đây là một chiến lược quan trọng trong dự phòng lây nhiễm chu sinh. Tuy vậy, quyết định dùng thuốc vẫn cần được cân nhắc kỹ giữa lợi ích điều trị và các nguy cơ tiềm ẩn. Trong quá trình điều trị, bác sĩ thường theo dõi sát chức năng thận và sức khỏe xương của người mẹ. Đồng thời, sau khi sinh, trẻ cũng nên được theo dõi định kỳ về sự phát triển thể chất và thần kinh để đảm bảo an toàn lâu dài. Nếu được chỉ định đúng và theo dõi đầy đủ, Tenofovir disoproxil fumarate vẫn được xem là một lựa chọn điều trị đáng tin cậy cho phụ nữ mang thai hoặc đang cho con bú trong kiểm soát viêm gan B.
Bên cạnh đó, nếu bạn muốn hiểu sâu hơn về các bệnh lý gan cũng như các kiến thức hữu ích về sức khỏe lá gan, hãy truy cập vào fanpage Bác Sĩ Lá Gan để cập nhật những thông tin y khoa chính thống cũng như các mẹo bảo vệ sức khỏe.
Câu hỏi thường gặp về Tenofovir disoproxil fumarate ở phụ nữ mang thai
Tenofovir có gây dị tật thai nhi không?
Các nghiên cứu hiện nay cho thấy không có bằng chứng Tenofovir làm tăng nguy cơ dị tật bẩm sinh so với dân số chung. Thuốc được xem là một trong những lựa chọn an toàn nhất trong điều trị HBV ở phụ nữ mang thai.
Có nên ngừng Tenofovir khi phát hiện mang thai?
Bệnh nhân không nên tự ý ngừng thuốc. Việc dừng điều trị đột ngột có thể gây bùng phát viêm gan và tăng nguy cơ lây truyền HBV cho thai nhi. Quyết định điều trị cần được thảo luận với bác sĩ chuyên khoa.
Dùng Tenofovir có thể cho con bú không?
Phụ nữ đang dùng Tenofovir vẫn có thể cho con bú vì lượng thuốc bài tiết vào sữa mẹ rất thấp và không gây ảnh hưởng đáng kể đến trẻ.
Số lần xem: 111